Krónika
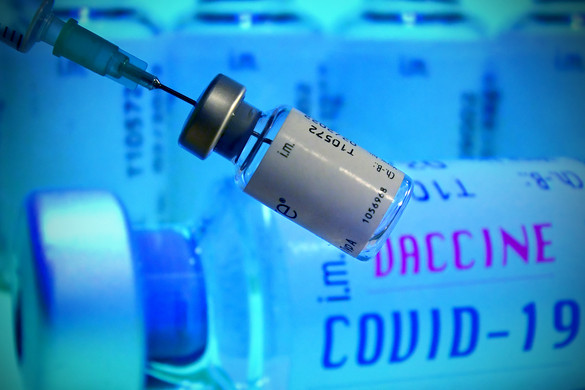
A Sputnik-V vakcina akár engedélyezés előtt is beadható
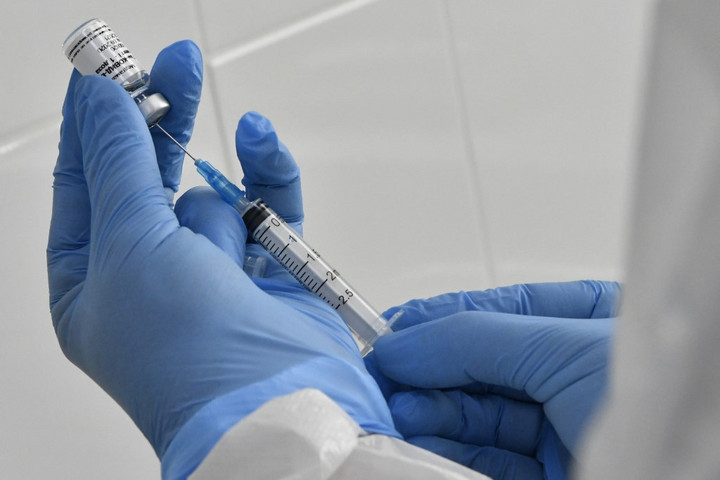
Központosított, nemzeti, kölcsönös elismerési- és decentralizált eljárással. Az utóbbi hárommal elvileg kikerülhető lenne az egységes, európai szintű engedélyeztetés, azonban a központosított eljárás kötelező a legtöbb innovatív gyógyszer esetén. Ebbe a kategóriába tartozik a koronavírus-vakcinák többsége, ahogy valószínűleg a Szputnyik–V is. A központosított eljárás tehát aligha kerülhető ki – fogalmazott.
A központosított eljáráson áteső gyógyszereket az Európai Gyógyszerügynökség (EMA) értékeli, majd forgalmazásukat az Európai Bizottság engedélyezi. Oroszország nem ezt az utat választotta, az EMA helyett az Egészségügyi Világszervezettel (WHO) vette fel a kapcsolatot. A vakcinát a gyártó szerint jelenleg több EU-n kívüli, úgynevezett harmadik államban (Oroszországban, Fehéroroszországban, Indiában, Venezuelában és az Egyesült Arab Emirátusokban) több ezer beteg részvételével zajló, úgynevezett harmadik (és egyben utolsó) fázisú klinikai vizsgálatoknak vetik alá, amelyet a WHO szakmai szempontból is figyelemmel kísér.
Mindazonáltal a WHO esetleges jövőbeni ajánlása, jóváhagyása nem válthatják ki a vakcina iránt érdeklődő országok forgalomba hozatali engedélyeit – mondta Novák Zoltán. Hozzátette, egyelőre itthon legfeljebb szigorúan ellenőrzött klinikai vizsgálatok folytathatók, melyekbe nagy számú „önkéntes” beteg is bevonható.
Az anyagból egyebek mellett az is kiderül, mivel a jelen kivételes helyzetben még az EU gyorsított eljárása sem feltétlenül elegendő a vírus elleni hatékony küzdelemhez, a tagállamoknak nem kell megvárniuk az eljárás végét, a forgalomba hozatali engedély kibocsátását, hanem egyéni döntésük alapján rendelkezhetnek bizonyos gyógyszerek engedélyezés előtti alkalmazásáról is.
Ez azt jelenti, hogy egy új gyógyszert kivételes okokból hozzáférhetővé tehetnek olyan betegek számára, akik krónikus vagy maradandó károsodást okozó betegségben szenvednek, vagy akiknek a betegsége életet veszélyeztető, és akik engedélyezett gyógyszerrel kielégítő módon nem kezelhetők.
Ez a feltétel teljesülhet a COVID-19 által fokozottan veszélyeztetett, krónikus betegségben szenvedők esetén, akik számára ezért a Sputnik-V vakcina akár engedélyezés előtt is beadható. Az érintett gyógyszernek azonban ebben az esetben is legalább benyújtott forgalomba hozatali engedély iránti kérelemmel vagy folyamatban lévő klinikai vizsgálattal kell bírnia.