Belföld
Versenyelőny a gyógyszerkutatásban
Egyértelművé teszi a klinikai vizsgálatokhoz szükséges szerződéseket az új rendelkezés, így a folyamatok felgyorsulhatnak
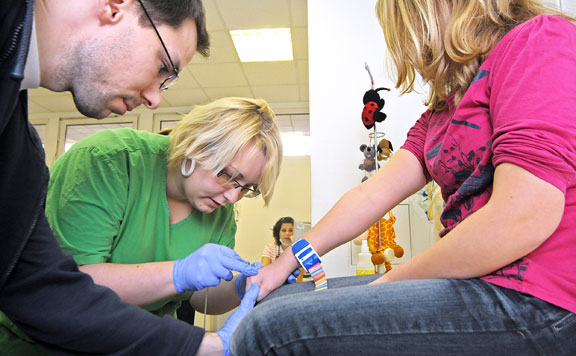
Az innováció erősítése a betegek érdekeit szolgálja a gyógyszergyártók szerint (képünk illusztráció) (Fotó: Varga Imre)
Egységes szerződésmintát vezetnek be ősztől a magyarországi klinikai vizsgálatoknál – közölte tegnap Ónodi-Szűcs Zoltán, aki elmondta azt is, az új szabályozás – a gyógyításra szánt hatóanyag tulajdonságainak, hatásainak feltárását célzó – klinikai vizsgálatokhoz szükséges dokumentumokat rendezi az illetékes cég és az ellátó között a korábbi, intézményenkénti szerződéseket kiváltva. Az egészségügyért felelős államtitkár jelezte, az Állami Egészségügyi Ellátó Központ (ÁEEK) olyan szabályozást léptet életbe, amely egyértelművé teszi az említett szerződéseket, így a folyamatok felgyorsulhatnak, amely a remények szerint azt eredményezi, hogy több klinika vizsgálatot lehet majd elvégezni Magyarországon.
Minden olyan törekvés, amely a hazai innovációt erősíti, a betegek érdekét szolgálja – közölte Ilku Lívia, a Magyarországi Gyógyszergyártók Országos Szövetségének (MGYOSZ) igazgatója, majd kitért arra is, hogy kutatási-fejlesztési tevékenységgel kétezer ember foglalkozik különböző tagvállalatoknál, így tavaly százhetvenkilenc új gyógyszerrel tudtak piacra lépni. „Az elmúlt éveket tekintve ez messze kimagasló eredménynek számít” – hangsúlyozta az MGYOSZ vezetője a távirati iroda tudósítása szerint.
Az Élelmezés-egészségügyi Intézet főigazgatója kijelentette, „Magyarország hosszú évek óta jó és kívánatos terep a nemzetközi gyógyszerkutatatások területén, amelyhez a hatósági munka is nagyban hozzájárult”. Pozsgay Csilla jelezte azt is, hogy 2018-ban megváltozik az Európai Unióban a klinikai vizsgálatokra vonatkozó hivatalos engedélyeztetési eljárás, ám azzal, hogy hazánk egyszerűsítette a felek közötti szerződéskötés menetét, „versenyelőnyre tett szert” a többi tagállammal szemben.
Németh László, az ÁEEK főigazgatója a tájékoztatón arról számolt be, hogy a most ismertetett változtatás „egyenlő és átlátható feltételeket teremt a klinikai vizsgálatot kezdeményező gyógyszercég és a kórház között”, ezenfelül pedig adatbázissal is segíti majd a munkát és a betegek tájékoztatását.
Thomas Straumits, az Innovatív Gyógyszergyártók Egyesületének (AIPM) elnöke arról beszélt, Magyarország a klinikai vizsgálatok számát tekintve Európában az első tíz ország között van. Az egységes szabályozás kialakításával további huszonöt-harminc százalékos bevételemelkedés érhető el a klinikai vizsgálatok révén, továbbá az intézkedés növeli Magyarország versenyképességét, és az ország további részt vállalhat a nemzetközi gyógyszerkutatásokban – vélekedett a szervezet elnöke.
Az AIPM beszámolója alapján a hazai intézményekben folyó gyógyszerkipróbálások kilencvenmilliárd forintot hoznak a nemzetgazdaságnak, húszezer beteg jut új gyógyszerekhez, innovatív terápiához, és kap esélyt a gyógyulásra. Hazánk „study nagyhatalom”, évente háromszáznál több új vizsgálat indul, a klinikai kipróbálások lakosságarányos számát tekintve a negyedik helyen állunk Európában. Álláspontjuk szerint „a versenyelőny a gyors hatósági ügyintézésnek és a költséghatékonyságnak köszönhető, ám van tennivaló annak érdekében, hogy ezt az előnyt meg is őrizzük”.